Die Duchenne-Muskeldystrophie (DMD) ist eine schwere (und die häufigste) Form der Muskeldystrophie, die vor allem Jungen betrifft. Die Muskelschwäche beginnt in der Regel um das vierte Lebensjahr und verschlimmert sich schnell. Der Muskelverlust tritt typischerweise zuerst in den Oberschenkeln und im Becken auf, gefolgt von den Armen.
Die Erkrankung ist X-chromosomal rezessiv. Etwa zwei Drittel der Fälle werden von der Mutter vererbt, während ein Drittel der Fälle auf eine neue Mutation zurückzuführen ist. Sie wird durch eine Mutation im Gen für das Protein Dystrophin verursacht. Dystrophin ist wichtig, um die Zellmembran der Muskelfasern aufrechtzuerhalten.
Symptomatik und Verlauf
DMD (auch Muskeldystrophie Duchenne) verursacht eine fortschreitende Muskelschwäche durch den Abbau von Muskelfasern. Zuerst sind die willkürlichen Muskeln betroffen, vor allem die der Hüften, des Beckenbereichs, der Oberschenkel und der Waden. Schließlich schreitet die Krankheit zu den Schultern und dem Nacken fort, gefolgt von den Armen, den Atemmuskeln und anderen Bereichen. Müdigkeit ist häufig.
Die Anzeichen treten normalerweise vor dem fünften Lebensjahr auf und können sogar von dem Moment an beobachtet werden, in dem ein Junge seine ersten Schritte macht. Es gibt allgemeine Schwierigkeiten mit der Motorik, was zu einer ungeschickten Art zu gehen, zu treten oder zu laufen führen kann. Sie neigen dazu, auf den Zehen zu gehen, zum Teil aufgrund der Verkürzung der Achillessehne, und weil sie die Schwäche der Kniestrecker kompensiert. Stürze können häufig vorkommen. Es wird für den Jungen immer schwieriger zu gehen. Ab dem 13 Lebensjahr ist er m Wesentlichen vom Hals abwärts gelähmt. Eine Kardiomyopathie ist häufig und wird bei der Hälfte der 18-Jährigen beobachtet. Die Entwicklung einer kongestiven Herzinsuffizienz oder Arrhythmie (unregelmäßiger Herzschlag) ist nur gelegentlich.
Ein klassisches Zeichen für DMD ist die Schwierigkeit, aus einer liegenden oder sitzenden Position aufzustehen, was sich durch ein positives Gowers-Zeichen manifestiert. Wenn ein Kind versucht, aus der Bauchlage aufzustehen, kompensiert es die Schwäche der Beckenmuskulatur durch den Einsatz der oberen Extremitäten:
zuerst durch Aufstehen, um auf seinen Armen und Knien zu stehen, und dann durch "Gehen" seiner Hände auf seinen Beinen, um aufrecht zu stehen.
Ein weiteres charakteristisches Zeichen für DMD ist die Pseudohypertrophie (Vergrößerung) der Muskeln der Zunge, der Waden, des Gesäßes und der Schultern (etwa im Alter von 4 oder 5 Jahren). Das Muskelgewebe wird schließlich durch Fett und Bindegewebe ersetzt, daher der Begriff Pseudohypertrophie. Es können Muskelfaserdeformationen und Muskelkontrakturen der Achillessehne und der Hamstrings auftreten, die die Funktionalität beeinträchtigen, weil sich die Muskelfasern verkürzen und in Bindegewebe einfasern. Es können Skelettdeformationen auftreten, wie lumbale Hyperlordose, Skoliose, vordere Beckenkippung und Brustkorbdeformationen. Es wird angenommen, dass die lumbale Hyperlordose ein kompensatorischer Mechanismus als Reaktion auf die Schwäche der Gesäß- und Quadrizepsmuskeln ist, die alle eine veränderte Körperhaltung und einen veränderten Gang (z. B. eingeschränkte Hüftstreckung) verursachen.
Es treten auch nicht-muskuloskelettale Manifestationen der DMD auf. Es besteht ein erhöhtes Risiko für neurologische Verhaltensstörungen (z.B. ADHS), Lernstörungen (Legasthenie) und nicht-progressive Schwächen in bestimmten kognitiven Fähigkeiten (insbesondere verbales Kurzzeitgedächtnis), von denen angenommen wird, dass sie das Ergebnis von fehlendem oder dysfunktionalem Dystrophin im Gehirn sind.
Ursache
Physiologie
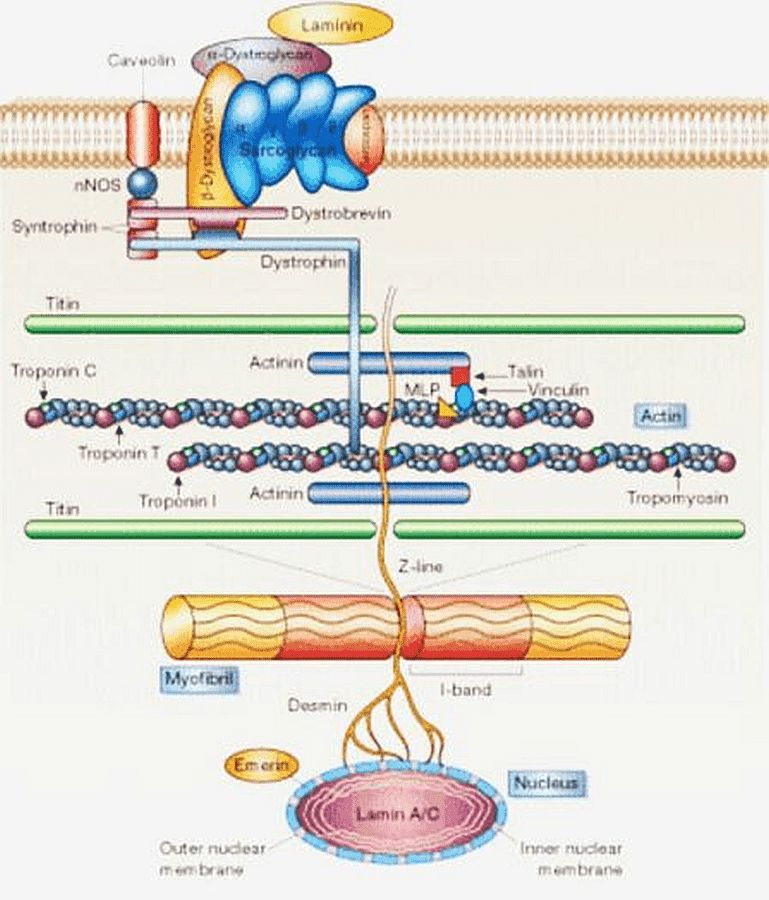
DMD wird durch eine Mutation des Dystrophin-Gens am Locus Xp21 verursacht. Dystrophin fungiert intrazellulär als Bindeglied zwischen Aktinfilament und beta-Dystroglycan. Das Fehlen von Dystrophin ermöglicht das Eindringen von überschüssigem Kalzium. Dies führt zum Eindringen von Wasser in die Mitochondrien, die dann platzen. Die Muskelfasern nekrotisieren und werden schließlich durch Fett- und Bindegewebe ersetzt.
Genetik
DMD wird in einem X-chromosomal-rezessiven Muster vererbt. Frauen sind typischerweise Träger des genetischen Merkmals (auf dem kurzen Arm des X-Chromosoms), während Männer betroffen sind. Eine weibliche Trägerin ist sich nicht bewusst, dass sie eine Mutation trägt, bis sie einen betroffenen Sohn hat. Der Sohn einer Trägermutter hat eine 50%ige Chance, das defekte Gen von seiner Mutter zu erben. Die Tochter einer Trägermutter hat eine 50%ige Chance, Trägerin zu sein und eine 50%ige Chance, zwei normale Kopien des Gens zu haben.
In allen Fällen gibt ein nicht betroffener Vater entweder ein normales Y an seinen Sohn oder ein normales X an seine Tochter weiter. Weibliche Träger einer X-chromosomal rezessiven Erkrankung, wie DMD, können Symptome zeigen, abhängig von ihrem Muster der X-Inaktivierung.
Häufigkeit
DMD betrifft etwa einen von 3.500 bis 6.000 Männern bei der Geburt. Es ist die häufigste Form der Muskeldystrophie. Die durchschnittliche Lebenserwartung liegt bei 26 Jahren; bei hervorragender Pflege können einige jedoch bis in ihre 30er oder 40er Jahre leben.
DMD ist bei Frauen extrem selten (etwa 1 von 50.000.000 weiblichen Geburten). Sie kann bei Frauen mit einem betroffenen Vater und einer Überträgermutter auftreten, bei solchen, denen ein X-Chromosom fehlt, oder bei solchen, die ein inaktiviertes X-Chromosom haben (die häufigste der seltenen Ursachen). Die Tochter einer Trägermutter und eines betroffenen Vaters wird mit gleicher Wahrscheinlichkeit betroffen oder eine Trägerin sein, da sie immer das betroffene X-Chromosom von ihrem Vater erbt und eine 50%ige Chance hat, auch das betroffene X-Chromosom von ihrer Mutter zu erben.
Diagnose
Eine genetische Beratung wird für Menschen mit einer Familienanamnese der Erkrankung empfohlen. DMD kann durch genetische Untersuchungen, die während der Schwangerschaft durchgeführt werden, mit einer Genauigkeit von etwa 95 % nachgewiesen werden. Die Kreatinkinase (CPK-MM)-Spiegel im Blut sind extrem hoch. Eine Elektromyographie (EMG) zeigt, dass die Schwäche durch die Zerstörung von Muskelgewebe und nicht durch eine Schädigung der Nerven verursacht wird.
DNA-Test
Die muskelspezifische Isoform des Dystrophin-Gens besteht aus 79 Exons, und ein DNA-Test (Bluttest) und eine Analyse können in der Regel den spezifischen Mutationstyp des betroffenen Exons oder der betroffenen Exons identifizieren. Der DNA-Test bestätigt die Diagnose in den meisten Fällen.
Muskelbiopsie
Wenn der DNA-Test die Mutation nicht findet, kann ein Muskelbiopsietest durchgeführt werden. Mit einer Biopsienadel wird eine kleine Probe des Muskelgewebes entnommen. Die wichtigsten Tests, die an der Biopsieprobe für DMD durchgeführt werden, sind Immunhistochemie, Immunzytochemie und Immunblotting für Dystrophin und sollten von einem erfahrenen neuromuskulären Pathologen interpretiert werden. Diese Tests liefern Informationen über das Vorhandensein oder Fehlen des Proteins. Die Abwesenheit des Proteins ist ein positiver Test für DMD. Wenn Dystrophin vorhanden ist, zeigen die Tests die Menge und die molekulare Größe des Dystrophins an und helfen so, DMD von milderen Dystrophinopathie-Phänotypen zu unterscheiden. In den letzten Jahren wurden DNA-Tests entwickelt, die mehr der vielen Mutationen nachweisen, die die Krankheit verursachen, und eine Muskelbiopsie ist nicht mehr so oft erforderlich, um das Vorhandensein von DMD zu bestätigen.
Pränatale Tests
Pränatale Tests (wenn die Mutter eine bekannte oder vermutete Trägerin ist) können feststellen, ob das ungeborene Kind eine der häufigsten Mutationen hat. Viele Mutationen sind für DMD verantwortlich, und einige sind noch nicht identifiziert worden, so dass Gentests fälschlicherweise negativ sein können, wenn die vermutete Mutation in der Mutter nicht identifiziert worden ist.
Vor einem invasiven Test ist die Bestimmung des fetalen Geschlechts wichtig; während Männer manchmal von dieser X-chromosomalen Krankheit betroffen sind, ist weibliche DMD extrem selten. Dies kann durch eine Ultraschalluntersuchung in der 16. Woche oder neuerdings auch durch einen kostenlosen fetalen DNA-Test erreicht werden. Die Chorionzottenbiopsie (CVS) kann bei 11-14 Wochen durchgeführt werden und hat ein 1%iges Risiko einer Fehlgeburt. Eine Fruchtwasseruntersuchung kann nach 15 Wochen durchgeführt werden und birgt ein Risiko von 0,5 % für eine Fehlgeburt. Eine fetale Blutentnahme kann um die 18. Woche durchgeführt werden. Eine weitere Option bei unklaren genetischen Testergebnissen ist die fetale Muskelbiopsie.
Therapie
Eine Heilung ist nicht bekannt; die Behandlung zielt im Allgemeinen darauf ab, das Auftreten von Symptomen zu kontrollieren, um die Lebensqualität zu maximieren, die mit spezifischen Fragebögen gemessen werden kann, und umfasst:
Konventionell
- Kortiko-Steroide wie Prednisolon und Deflazacort führen zu kurzfristigen Verbesserungen der Muskelkraft und -funktion bis zu 2 Jahren. Es wurde auch berichtet, dass Kortikosteroide helfen, das Gehen zu verlängern, obwohl die Beweise dafür nicht robust sind.
- Randomisierte Kontrollstudien haben gezeigt, dass β2-Agonisten die Muskelkraft erhöhen, aber die Krankheitsprogression nicht verändern. Die Nachbeobachtungszeit für die meisten RCTs zu β2-Agonisten beträgt nur etwa 12 Monate, daher können die Ergebnisse nicht über diesen Zeitrahmen hinaus extrapoliert werden.
- Antikonvulsiva zur Kontrolle von Anfällen und einiger Muskelaktivitäten sowie Immunsuppressiva zur Verzögerung der Schädigung sterbender Muskelzellen
- Leichte, nicht erschütternde körperliche Aktivität wie Schwimmen wird empfohlen. Inaktivität (wie Bettruhe) kann die Muskelerkrankung verschlimmern.
- Physiotherapie ist hilfreich, um Muskelkraft, Flexibilität und Funktion zu erhalten.
- Orthopädische Hilfsmittel (wie Zahnspangen und Rollstühle) können die Mobilität und die Fähigkeit zur Selbstversorgung verbessern. Formschlüssige, abnehmbare Beinschienen, die den Knöchel während des Schlafs in Position halten, können das Auftreten von Kontrakturen verzögern.
- Eine angemessene Unterstützung der Atmung bei fortschreitender Erkrankung ist wichtig.
- Herzprobleme können einen Herzschrittmacher erforderlich machen.
Gentherapie
Das Medikament Eteplirsen, ein Morpholino-Antisense-Oligo, wurde in den USA für die Behandlung von Mutationen zugelassen, die zum Skippen des Dystrophin-Exons 51 führen. Die US-Zulassung war umstritten, da Eteplirsen keinen klinischen Nutzen nachweisen konnte; die Europäische Arzneimittelbehörde verweigerte ihm die Zulassung.
In der EU ist das Medikament Ataluren (Translarna) zugelassen. Die Interaktion von Ataluren und dem Ribosom bewirkt, dass anstelle des Stopp-Codons eine Aminosäure eingefügt wird. Dies ermöglicht es dem Ribosom, die Synthese von Dystrophin-mRNA weiter fortzusetzen. Auf diese Weise kann das Zielprotein in geringen Mengen erzeugt werden.
Physikalische Therapie
Physiotherapeuten befassen sich damit, den Patienten zu ermöglichen, ihr maximales körperliches Potential zu erreichen. Ihr Ziel ist es:
- die Entwicklung von Kontrakturen und Deformitäten zu minimieren, indem sie ein Programm von Dehnungen und Übungen entwickeln, wo es angebracht ist
- andere sekundäre Komplikationen körperlicher Natur vorhersehen und minimieren, indem sie Stützvorrichtungen und dauerhafte medizinische Geräte empfehlen
- Überwachung der Atmungsfunktion und Beratung zu Techniken zur Unterstützung von Atemübungen und Methoden zur Sekretabsaugung
Geschichte
Die Krankheit wurde erstmals 1834 von dem neapolitanischen Arzt Giovanni Semmola und 1836 von Gaetano Conte beschrieben. Benannt ist die DMD jedoch nach dem französischen Neurologen Guillaume-Benjamin-Amand Duchenne (1806-1875), der in der 1861 erschienenen Ausgabe seines Buches "Paraplegie hypertrophique de l'enfance de cause cerebrale" den Fall eines Jungen beschrieb, der diese Erkrankung hatte. Ein Jahr später präsentierte er Fotos seines Patienten in seinem Album de photographies pathologiques. Im Jahr 1868 berichtete er über 13 weitere betroffene Kinder. Duchenne war der erste, der eine Biopsie durchführte, um Gewebe von einem lebenden Patienten für die mikroskopische Untersuchung zu gewinnen.
Siehe auch